
不知道你有没有这样的经历,如果是铜杯或者是铜管中的水,放的时间长了会有一股金属的味道,但是我们知道铜并不溶于水,并且也不像一些活泼金属那样能够和水起反应,那么这股金属味道是从何而来呢?
虽然纯铜确实不和纯水发生化学反应,但是要知道一般的水内部都含有杂质,这些杂质会使得铜能够和水发生缓慢的反应,这就是铜腐蚀的过程,最终会形成一种铜盐。
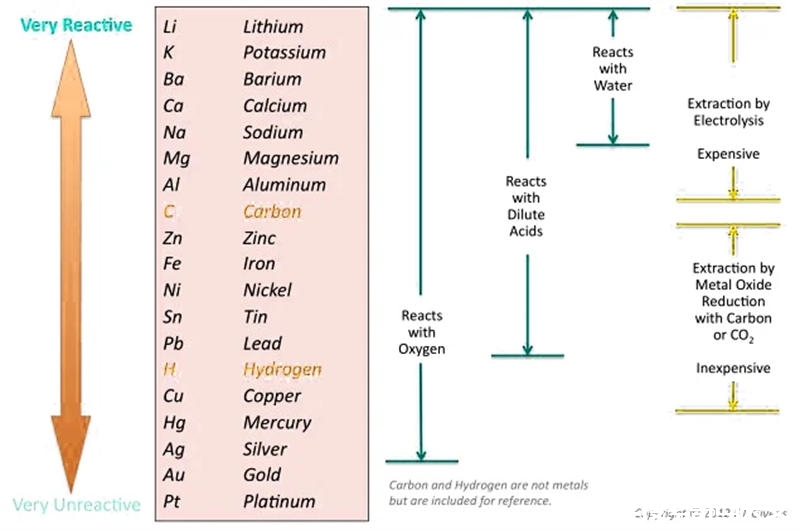
铜不是一种活泼的金属。在标准条件下,铜不能从水中置换氢。铜不通过置换反应与水发生反应,但它可以与水、氧气和污染物发生氧化还原/电化学反应,形成铜络合物。
铜腐蚀在未受污染的空气中可以忽略不计,但当暴露在与氧气和二氧化碳、氧化性酸、氧化性重金属盐、硫、氨等混合的水分中时,它很容易被腐蚀。

腐蚀既是一种氧化还原反应,也是一种电化学反应。在这些反应中,电子在两个离子或元素之间转移。
例如,在水的存在下,来自铁的电子移动到电负性更强的氧,形成带负电的氢氧根离子。带正电的铁首先与带负电的氢氧根离子反应生成氢氧化铁,氢氧化铁随后与氧气反应生成棕色片状水合氧化铁,称为铁锈。
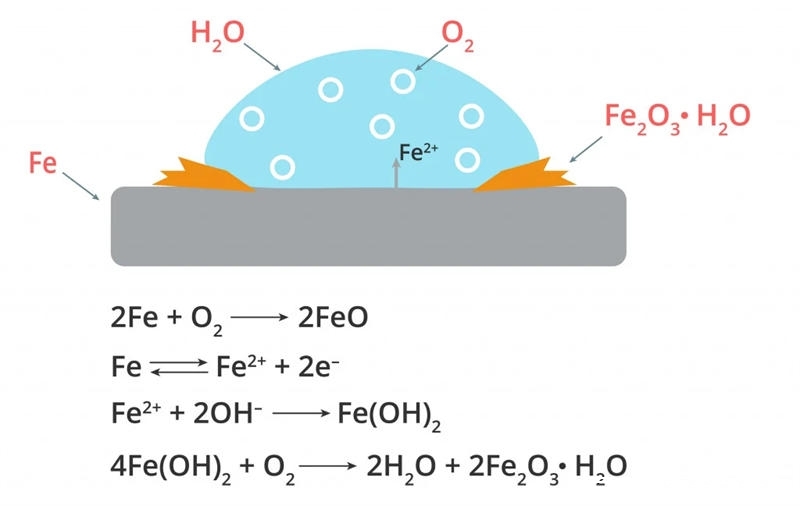
在这里,生锈过程首先涉及与水的反应,然后是与氧气的反应。
所有形式的腐蚀都是由氧化还原反应引起的,但反应产物变化多端:铁生锈中的水合氧化铁、银失去光泽中的硫化银和铜锈蚀中的碳酸铜。共同点是电子从金属转移到电负性原子。
铜锈通常被认为是迷人的,具有古董的感觉,但这种美丽的建筑和雕塑方面是基于铜表面形成的铜锈。然而,容器中的碳酸铜铜绿会让水产生一种金属味道。
第一步:电子从金属内部移动到外部的水分中。金属失去电子的区域为阳极区;
Cu(s) →Cu 2+ + 2e –
第二步:电子与氧气和水分反应生成氢氧化物;
O2(g) + 2H2O+ 4e– →4OH–
第三步:氢氧根阴离子向内移动与Cu2+反应生成氢氧化铜;
Cu2+ + 2OH – →Cu(OH)2
第四步:CO2与氢氧化铜反应生成碳酸铜,碳酸铜是铜绿的成分之一;
Cu(OH)2 + CO2 → CuCO3 + H2O
第五步:氧化铜还与三氧化硫污染物反应生成硫酸铜。
CuO + SO3 +H2O→ CuSO4 + H2O
铜绿是氢氧化铜、碳酸铜、氯化铜和硫酸铜的混合物。氢氧化铜和碳酸铜不溶于水,但硫酸铜和氯化铜适度进入水中,因此当水储存在这种腐蚀的铜容器或管道中时,会留下难闻的金属味。

铜的腐蚀在金属表面留下一层复杂的可溶性和不溶性铜盐。这用作防止下面的金属进一步腐蚀的保护层。然而,可溶性铜盐会微妙地溶解在容器中储存的水中,产生一种令许多人不愉快的金属味!

